이온 ion
목차
이온의 형성
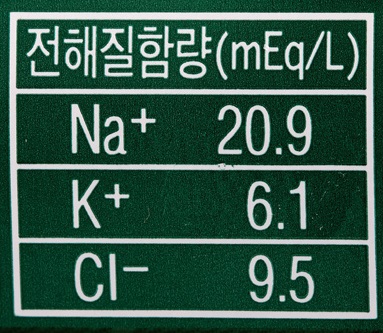
운동을 하고 나서 즐겨 마시는 음료 중에 이온 음료가 있다. 이온 음료에는 여러 가지 이온이 들어 있다. 이온이란 무엇일까?
이온은 원자로부터 만들어진다. 이온 음료에 들어 있는 이온 중 하나인 나트륨 이온은 나트륨 원자와 무엇이 다를까?
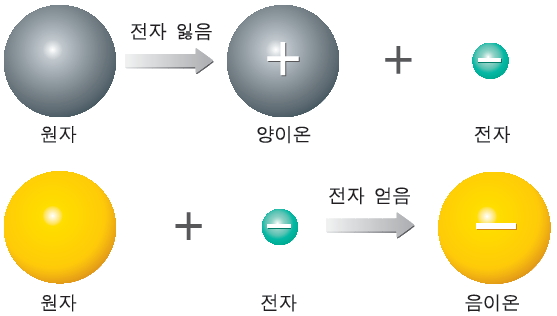
원자는 (+)전하를 띤 원자핵과 (-)전하를 띤 전자로 이루어져 있다. 원자핵 주위에 있는 전자들 중에는 다른 종류의 원자로 이동할 수 있는 것이 있다. 어떤 종류의 원자는 전자를 잃기 쉽고, 다른 종류의 원자는 전자를 얻기 쉽다. 중성인 원자가 전자를 잃거나 얻으면 전하를 띠며, 이렇게 전하를 띠는 입자를 이온이라고 한다.
중성인 원자가 전자를 잃어 (+)전하를 띠는 입자를 양이온이라고 하고, 중성인 원자가 전자를 얻어 (-)전하를 띠는 입자를 음이온이라고 한다.
※ 양이온의 형성
금속 원소는 양이온을 주로 형성한다. 금속 원소는 주기율표에서 주로 왼쪽에 위치하는 1, 2, 13족 원소들이다. 금속 원소는 최외각 전자 1~3개를 가지고 있으며, 이 전자 수만큼 전자를 잃어 +1~+3의 양이온을 형성하여 안정한 전자 배치를 이룬다.
* 1족 원소 : +1의 양이온 형성
예) Li+, Na+, K+
* 2족 원소 : +2의 양이온 형성
예) Mg2+, Ca2+
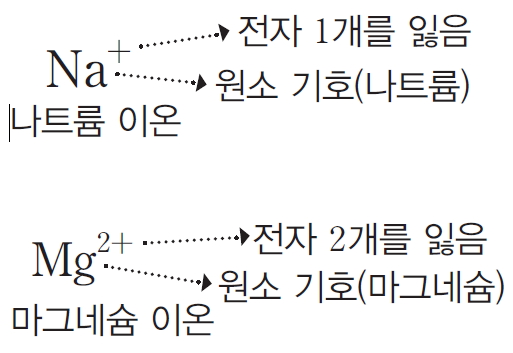
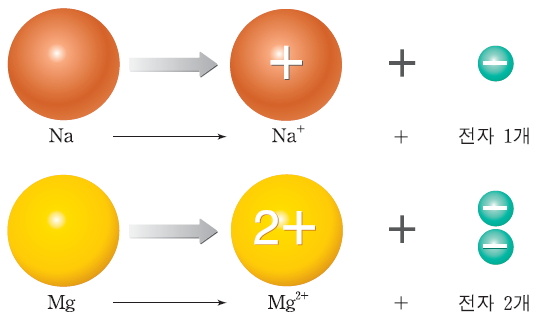
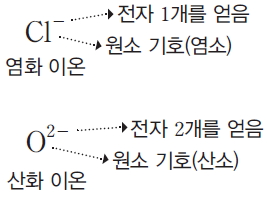
이온은 원소 기호를 이용하여 나타낸다. 원소 기호의 오른쪽 위에 전하의 종류와 잃거나 얻은 전자 수를 함께 나타낸다. 그림과 같이 원자가 전자를 1개 잃으면 +1의 양이온이 생성되고, 원자가 전자를 2개 잃으면 +2의 양이온이 생성된다.
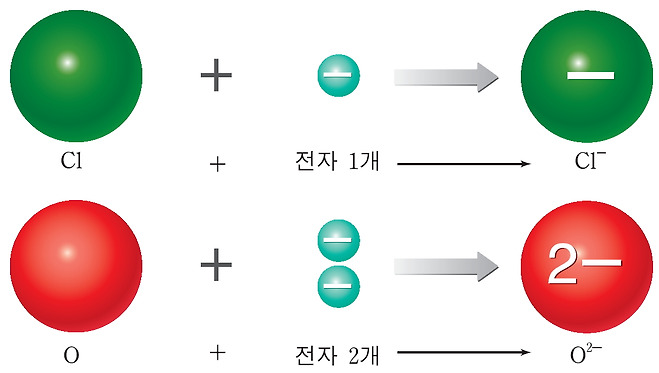
원자가 전자를 1개 얻으면 -1의 음이온이 생성되고, 원자가 전자를 2개 얻으면 -2의 음이온이 생성된다.
※ 음이온의 형성
비금속 원소는 음이온을 주로 형성한다. 비금속 원소는 주기율표에서 주로 오른쪽에 위치한다. 16, 17족 원소들이 대표적인 비금속 원소들인데, 이 원소들의 최외각 전자 수는 6~7개로 최외각 전자 8개를 이루기 위해 1~2개의 전자를 얻어 음이온을 형성하여 안정한 전자 배치를 이룬다.
* 16족 원소 : -2의 음이온 형성
예) O2-, S2-
* 17족 원소
예) F-, Cl-
이온의 이름을 부를 때에는 양이온의 경우 원소 이름 뒤에 ‘이온’을 붙여부른다. 음이온의 경우 보통 원소 이름 뒤에 ‘~화 이온’을 붙여 부른다.
이온 중에는 나트륨 이온(Na+)과 같이 1개의 원자로 이루어진 것도 있고, 수산화 이온(OH-), 탄산 이온(CO32-)과 같이 여러 원자로 이루어져 있는 상태에서 전하를 띠는 것도 있다.
| 양이온 | 이온식 | 음이온 | 이온식 |
| 수소 이온 | H+ | 염화 이온 | Cl- |
| 나트륨 이온 | Na+ | 산화 이온 | O2- |
| 칼륨 이온 | K+ | 황화 이온 | S2- |
| 은 이온 | Ag+ | 질산 이온 | NO3- |
| 칼슘 이온 | Ca2+ | 탄산 이온 | CO32- |
| 암모늄 이온 | NH4+ | 황산 이온 | SO42- |
* 음이온의 이름 : 음이온의 경우 ‘소’로 끝나는 산소와 염소는 ‘소’를 빼고 ‘~화 이온’을 붙여 산화 이온, 염화 이온으로 부른다.
* 다원자 이온 : 황산 이온(SO42-)은 황 원자 1개와 산소 원자 4개가 모여 -2의 음이온이 된다. 이처럼 여러 원자가 결합하여 전체가 양전하 또는 음전하를 띠는 이온을 다원자 이온이라고 한다.
예) 탄산 이온(CO32-), 질산 이온 (NO3-), 암모늄 이온(NH4+)
이온의 형성을 모형으로 나타내기
준비물
색도화지, 빨간색 스타이로폼 공(지름 4 cm), 초록색 스타이로폼 공(지름 2 cm), 가위, 펜, 컴퍼스, 양면테이프
과정
1. 색도화지를 잘라 지름이 20 cm인 원판 2개를 만든다.
2. 빨간색 스타이로폼 공 위에 + 3, + 9라고 쓰고, 과정 1에서 준비한 원판 중앙에 붙인다.
3. 초록색 스타이로폼 공 위에 -1이라고 쓰고, 원판 중앙의 숫자만큼 초록색 스타이로폼 공을 각각 올려놓아 리튬 원자와 플루오린 원자의 모형을 만든다.
→ 원자핵과 전자의 지름이 각 입자의 실제 크기를 나타내는 것은 아니다.
4. 리튬 원자 모형에서 초록색 스타이로폼 공 1개를 빼내어 플루오린 원자 모형에 올려놓아 리튬 이온과 플루오린화 이온의 모형을 만든다.
각 모형에서 빨간색 스타이로폼 공 위에 쓴 숫자와 초록색 스타이로폼 공 위에 쓴 숫자를 모두 더하면 얼마가 되는가?
리튬 원자 모형과 플루오린 원자 모형에서 각각 빨간색 스타이로폼 공 위에 쓴 숫자와 초록색 스타이로폼 공 위에 쓴 숫자를 모두 더하면 0이 된다.
각 모형에서 원판 중앙의 숫자와 초록색 스타이로폼 공에 쓴 숫자를 모두 더하면 얼마가 되는가?
리튬 이온 모형은 +1, 플루오린화 이온 모형은 -1이 된다.
[ 결과 및 정리 ] 1. 초록색 스타이로폼 공을 옮기기 전 리튬과 플루오린은 각각 어떤 전하를 띠는가?
정답 : 전하를 띠지 않는다. 원자핵의 (+)전하량과 전자의 전체 (-)전하량이 같아서 중성이다.
[ 결과 및 정리 ] 2. 초록색 스타이로폼 공 1개를 옮기면 리튬과 플루오린은 각각 어떤 전하를 띠는가?
리튬은 +1의 전하를 띠는 리튬 이온(Li+)이 되고, 플루오린은 -1의 전하를 띠는 플루오린화 이온(F-)이 된다.
[ 결과 및 정리 ] 3. 원자와 이온의 차이점을 설명해 보자.
원자는 원자핵의 (+)전하량과 전자의 전체 (-)전하량이 같아서 중성이지만, 이온은 중성의 원자가 전자를 잃거나 얻어서 전하를 띤 입자이다.
리튬 원자는 원자핵의 전하량이 +3이고, 전자의 전체 전하량이 -3이므로 전기적으로 중성이다. 그런데 리튬 원자가 전자 1개를 잃으면 (+)전하량이 많으므로 리튬 이온(Li+)이 된다. 또한, 플루오린 원자는 원자핵의 전하량이 +9이고, 전자의 전체 전하량이 -9이므로 전기적으로 중성이다. 그런데 플루오린 원자가 전자 1개를 얻으면 (-)전하량이 많으므로 플루오린화 이온(F-)이 된다.
간단한 화합물을 원소 기호로 나타내기
우리 주위에는 많은 물질이 있다. 이들 중에서 금이나 구리 등은 한 가지 원소로 이루어진 물질이고, 염화 나트륨이나 물 등은 두 가지 이상의 원소로 이루어진 물질이다. 염화 나트륨이나 물과 같이 두 가지 이상의 원소가 결합하여 생성된 물질을 화합물이라고 한다. 화합물은 어떻게 원소 기호로 나타낼 수 있을까?
염화 나트륨과 같이 이온으로 이루어진 화합물의 경우 양이온을 먼저 쓰고 음이온을 나중에 쓴 다음, 결합하는 양이온과 음이온의 개수 비를 구한다. 각 이온의 개수 비를 원소 기호의 오른쪽 아래에 작은 숫자로 표시하며, 1은 생략한다. 예를 들어 염화 칼슘이 생성될 때 칼슘 이온(Ca2+)과 염화 이온(Cl-)은 1 : 2로 결합한다. 이때 양이온의 전하량과 음이온의 전하량의 합은 0이 된다.
양이온의 전하량 : Ca2+의 개수와 전하량의 곱=1×(+2)=+2
음이온의 전하량 : Cl-의 개수와 전하량의 곱=2×(-1)=-2
따라서 염화 나트륨, 탄산 칼슘, 염화 마그네슘은 NaCl, CaCO3, MgCl2로 나타낼 수 있다. 그러면 이온으로 이루어지지 않은 화합물은 어떻게 원소 기호로 나타낼 수 있을까?
물, 이산화 탄소는 두 가지 이상의 원소가 결합한 화합물로 각각 H2O, CO2로 나타낸다. 즉 화합물을 구성하는 원소의 종류와 원자의 개수를 원소 기호로 나타낸다. 원자의 개수 비는 원소 기호의 오른쪽 아래에 작은 숫자로 표시하며, 1은 생략한다.
※ 공유 결합 화합물과 이온 결합 화합물
화합물을 이루는 원소들이 결합하는 방식은 크게 공유 결합과 이온 결합으로 구분할 수 있다.
공유 결합으로 만들어지는 화합물은 공유 결합 화합물, 이온 결합으로 만들어지는 화합물은 이온 결합 화합물로 구분할 수 있다. 대부분의 유기 화합물을 비롯하여 실온에서 기체나 액체로 존재하는 물질들은 공유 결합에 의해 형성되므로 공유 결합 화합물이라고 할 수 있다.
염화 나트륨, 염화 구리 등의 화합물은 양이온인 금속 이온과 음이온인 비금속 이온이 정전기적 인력에 의해 결합하므로 이온 결합 화합물이라고 할 수 있다.
※ 이온으로 이루어진 물질은 물에 녹인 다음 전류를 흘려주어야 이온으로 되나요?
서로 다른 두 원소가 결합하여 이온으로 이루어진 물질을 만들 경우 먼저 양이온과 음이온이 만들어지면서 이 두 이온이 결합한다. 그러므로 물에 녹지 않아도 이미 이온으로 이루어져 있다.
잠깐 퀴즈
1. 원자가 전자를 잃거나 얻어 전하를 띠는 입자를 무엇이라고 하는가?
정답 :이온
2. 이온이 형성되는 과정을 설명할 수 있는 모형을 고안해 보자.
예시 답안 | 강강술래에서는 사람들이 서로 손을 잡고 원을 돈다. 원을 도는 사람을 원자에서 전자에 비유하면, 원을 돌다가 사람들이 빠져나가면 양이온이 형성되는 것으로, 사람들이 더 들어오면 음이온이 형성되는 것으로 비유할 수 있다.
'사는 이야기 > 과학사전' 카테고리의 다른 글
| 가장 큰 별?..별 하나가 태양계 삼킨다 (0) | 2017.04.07 |
|---|---|
| 화합물 (0) | 2017.03.11 |
| 물 (0) | 2017.03.11 |
| 이온 결합 화합물의 물에 대한 용해성 (0) | 2017.03.11 |
| 아날로그와 디지털의 차이 (0) | 2017.02.08 |